اوربیتال اتمی تابع ریاضی است که رفتار موجی مانند یک الکترون و یا یک جفت الکترون در اتم را توضیح میدهد. این تابع را میتوان به منظور محاسبهٔ احتمال حضور الکترون در یک اتم در مناطق خاصی در اطراف هسته مورد استفاده قرار داد. از عملکرد این تابع میتواند در ترسیم نمودار سه بعدی از احتمال حضور الکترون در یک مکان استفاده کرد که این منطقهٔ فیزیکی با احتمال زیاد تعیین میشود. به طور خاص، اوربیتالهای اتمی ممکن در ویژه حالتی از یک تک الکترون که در مجموعهای از الکترونها در اطراف اتم منفرد قرار دارند با تابع اوربیتال توضیح داد.
اوربیتال اتمی را که در آن الکترون به عنوان ذرات جامد است، هرگز نمیتوان با سیارهٔ که بصورت بیضوی به دور خورشید میگردد توضیح داد.
با یک مقایسه دقیق ممکن است چنین به نظر برسد که الکترونی که درجو اطراف هسته قرار دارد مانند جو یک سیارهاست. اوربیتال اتمی نحوه شکل گیری این جو را فقط به یک الکترون منفرد در یک اتم را توضیح میدهد. وقتی که الکترونهای بیشتری به اتم منفرد اضافه میشود این الکترونها تمایل دارند بطور مساوی در حجم فضای اطراف هسته قرار بگیرند (که گاهی به این ابر الکترونی) گفته میشود.)این منطقه معمولاً کروی شکل است.
این ایده که الکترون ممکن است در اطراف هسته با یک خاصیت چرخشی که به آن تکانهٔ زاویهای میگویند میگردد، در سال ۱۹۱۳ توسط نیلز بور استدلال شد. و یک فیزیکدان ژاپنی به نام هانتارو ناگااٌکا(Hantaro Nagaoka) در اوایل سال ۱۹۰۴ فرضیه مبتنی به رفتارهای الکترونیکی به این مورد را منتشر کرد.. با این حال تا سال ۱۹۲۶ معادله شرودینگر برای حل حرکت موجی الکترون در اتم برای توابع اوربیتال جدید آماده نبود..
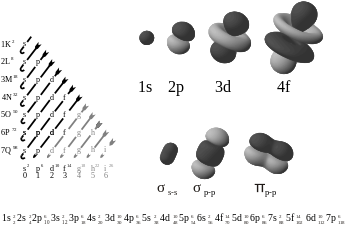
با توجه به تفاوت مدارمکانیک کلاسیک از واژه «مدار» برای الکترون در اتم، برای اولین بارشیمیدانی بنام رابرت میلیکان در سال ۱۹۳۲ اصطلاح اوربیتال را ابداع و جایگزین آن کرد.. اوربیتال اتمی، معمولاً به عنوان توصیف هیدروژنگونه (به معنی یک الکترون) برای تابع موج در فضا است، اعداد کوانتومی که بصورت l,nوm دسته بندی میشوند به ترتیب متناظر هستند با انرژی جفت الکترون ، تکانه زاویهای و تکانه زاویهای مسیر (بردار اقلیدسی تکانه زاویهای). هر اوربیتال (توسط یک مجموعه از اعداد کوانتومی متفاوت تعریف میشود) که دارای حداکثر دو الکترون است، از نامهای کلاسیک در آرایش الکترونی نشان داده شده در تصویر سمت چپ نیزاستفاده شدهاست. نامهای اوربیتال کلاسیک که با (s، p، d، f) نشان داده میشوند از ویژگیهای خطوط طیفی آنها مشتق شدهاست. در واقع این نامها را در تحلیل طیف گسیلی خطی فلزات قلیایی وضع کردند که f,d,p,s به ترتیب برگرفته از واژههای انگلیسی fundamental,diffuse,principal,sharp میباشند..
از حدود سال ۱۹۲۰، یا حتی قبل از ظهور مکانیک کوانتومی مدرن، اصل آفبا (اصل ساخت و ساز) است که در آن اتمها متشکل از جفت الکترونهای هستند، که از تکرار یک الگوی ساده و منظم که با افزایش اعداد فرد (.. ۱، ۳، ۵، ۷) است پیروی میکنند، توسط نیلز بور و دیگران که برای پی بردن به وجود چیزی شبیه به اوربیتال اتمی، در داخل تعدادی از ساختار الکترونی اتمهای پیچیده مورد استفاده قرار گرفته بود. در ریاضیات فیزیک اتمی، برای ساده کردن تابع موج الکترون در سیستمهای پیچیده اغلب مناسب از ترکیبات ساده تر اوربیتال اتمی استفاده شود. اگرچه هر الکترون را نمیتوان در یک اتم چند الکترونی که یکی را از یک یا دوالکترون ازاوربیتال اتمی در یک تصویر خیالی محدود کرد، هنوز هم تابع موج الکترون ممکن است ترکیباتی از اوربیتال اتمی را دربر داشته باشد؛ مثل اینکه، در بعضی مواقع ابر الکترونی یک اتم چند الکترونی هنوز هم با اوربیتال اتمی متشکل از تنها یک یا دو الکترون باشد.
ویژگیهای الکترون
پس از گسترش یافتن مکانیک کوانتوم به این حقیقت پی برده شد که الکترونهای در حال گردش در اطراف هسته را نمیتوان به طور کامل به شکل ذرات توصیف کرد بلکه میبایست با مفهوم دوگانگی موج-ذره توصیف شوند. از این نقطه نظر الکترون دارای ویژگیهای زیر است: ویژگیهای موج گون: ۱)چرخش الکترونها پیرامون هسته نه به شکل چرخش سیارات پیرامون خورشید بلکه به شکل یک موج ایستاده میباشد؛ بنابراین پایینترین انرژی که یک الکترون میتواند دارا باشد متناظر با بسامد اصلی یک موج ایستاده روی یک ریسمان است. انرژیهای ممکن بالاتر متناظر با سایر هماهنگهای بسامد اصلی خواهد بود. ۲)الکترونها در یک مکان نقطهای تنها نیستند، اگرچه احتمال برهمکنش با الکترون در یک نقطه مشخص میتواند از روی تابع موج الکترون محاسبه شود. ویژگیهای ذره گون: ۱)همواره شمار الکترونهای در حال گردش پیرامون هسته عددی صحیحی است. ۲)الکترونها بین اوربیتالها جهش میکنند. در این جهشها به نوعی رفتار ذرهای الکترون مشهود است. به عنوان مثال اگر یک تک فوتون الکترونها را تحریک کند صرفاً یک الکترون در پاسخ به این فوتون در تراز انرژی خود تغییر صورت میدهد. ۳)الکترونها خواص ذره گونی از قبیل این که هر حالت موجی همان بار الکتریکی ذره الکترون را دارد و یا این که هر حالت موجی دارای یک تک اسپین است. (اسپین رو به بالا یا پایین) را حفظ میکنند؛ بنابراین به رغم شباهت آشکار بحث ما با موضوع سیارات در حال گردش پیرامون خورشید، الکترونها نمیتوانند به سادگی به صورت ذراتی جامد توصیف شوند. به علاوه، اوربیتالهای اتمی شباهت نزدیکی با مدارهای فضایی چرخش سیارات به دور خورشید ندارند. یک شباهت دقیق تر میتواند این باشد که یک جو بزرگ و غالباً عجیب (الکترونها) سیارهای نسبتاً کوچک (هسته اتم) را احاطه کرده است. اوربیتالهای اتمی به طور دقیق شکل این «جو الکترونی» را توصیف میکنند به شرط آن که یک تک الکترون در اتم وجود داشته باشد. هنگامی که الکترونهای بیش تر به یک اتم افزوده میشوند، الکترونهای اضافه شده حجمی از فضا که پیرامون هسته است را چنان اشغال میکنند که مجموعه حاصل-که بعضی موارد «ابرالکترونی» نامیده میشود-شکل یک توزیع نسبتاً کروی را به خود میگیرد که الکترونها میتوانند در آن جا یافت شوند.
